2024年11月26日,同济大学附属上海市第四人民医院熊利泽团队在British Journal of Anaesthesia 在线发表题为“Structural Basis for the Inhibition of Cystathionine-β-Synthase by Isoflurane and Its Role in Anaesthesia-induced Social Dysfunction”的研究论文,该研究报道,吸入麻醉药异氟烷通过直接结合抑制胱硫醚-β-合成酶(CBS)活性,导致前扣带皮层(ACC)锥体神经元活动减弱,从而在成年和老年小鼠中引发社交功能障碍。
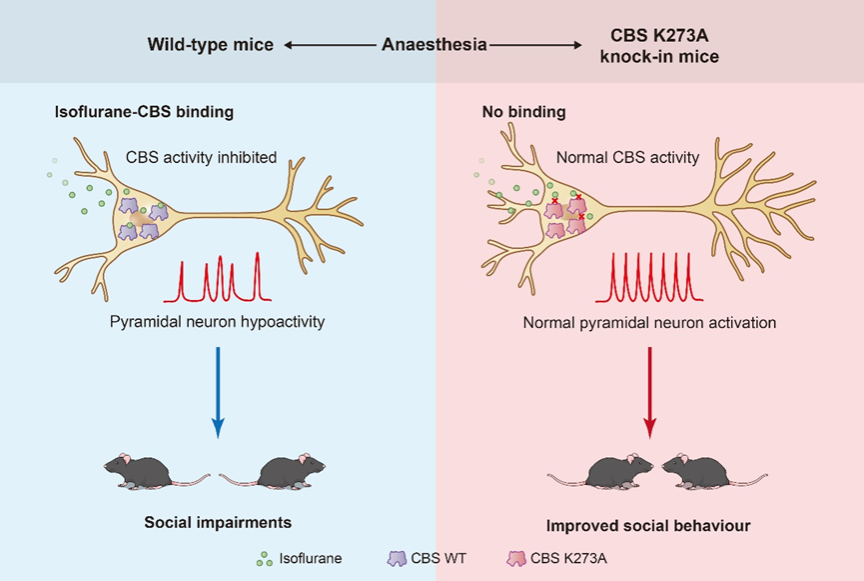
CBS在社交行为的调控中发挥重要作用,异氟烷通过结合CBS的关键氨基酸残基抑制其催化活性,进而影响社交互动中神经元的激活,导致社交功能受损。通过点突变阻断CBS与异氟烷的结合,有效改善了麻醉后CBS的活性,恢复了ACC神经元的激活以及小鼠的社交功能。综上,该研究揭示了异氟烷抑制CBS活性的结构基础,阐明了这种相互作用是导致社交障碍的关键因素,为深入理解麻醉引发的神经功能损伤提供了重要的分子层面解释。

社交功能下降是麻醉手术后常被忽视的并发症。据报道,约18.3%-31.2%的成年及老年患者术后出现社交功能障碍。这种功能减退不仅诱发焦虑和抑郁等情感障碍,还可能在某些特定人群中加重已有的认知功能损伤,严重影响生活质量。异氟烷作为一种常用的吸入麻醉药,近年来被发现对神经发育具有潜在损害作用,且越来越多的证据表明其在新生动物及儿童中介导社交缺陷。然而,关于异氟烷对成年和老年患者或动物社交功能的影响及其潜在机制,相关研究依然匮乏。
本研究发现,成年小鼠和老年小鼠接受异氟烷麻醉后,ACC脑区神经元在社交行为测试中的激活减弱,并表现出显著的社交功能下降。同时,麻醉后ACC内CBS活性被显著抑制,而在麻醉前进行CBS变构激活剂给药,可改善异氟烷麻醉介导的CBS活性下降,从而恢复ACC的神经元活动和社交功能。进一步的实验表明,CBS抑制剂给药诱导出与异氟烷麻醉后类似的现象,即ACC神经元活性降低和社交行为缺陷。这些结果提示异氟烷抑制CBS活性是影响社行为的重要原因。为了深入探究内在机制,作者通过X射线晶体学技术解析了CBS与异氟烷的结合位点。异氟烷与CBS催化核心域第276位精氨酸残基直接结合,是抑制其活性的结构基础。据此,作者构建了这一点突变敲入(KI)的转基因小鼠,有效地保护了异氟烷麻醉后的CBS活性。相较于野生型对照小鼠,KI小鼠在麻醉后表现出正常的ACC神经元激活水平,社交功能也被有效改善。因此,本研究通过结构生物学技术结合新品系转基因小鼠,揭示并验证了异氟烷结合并抑制CBS活性是介导社交障碍的重要上游机制。
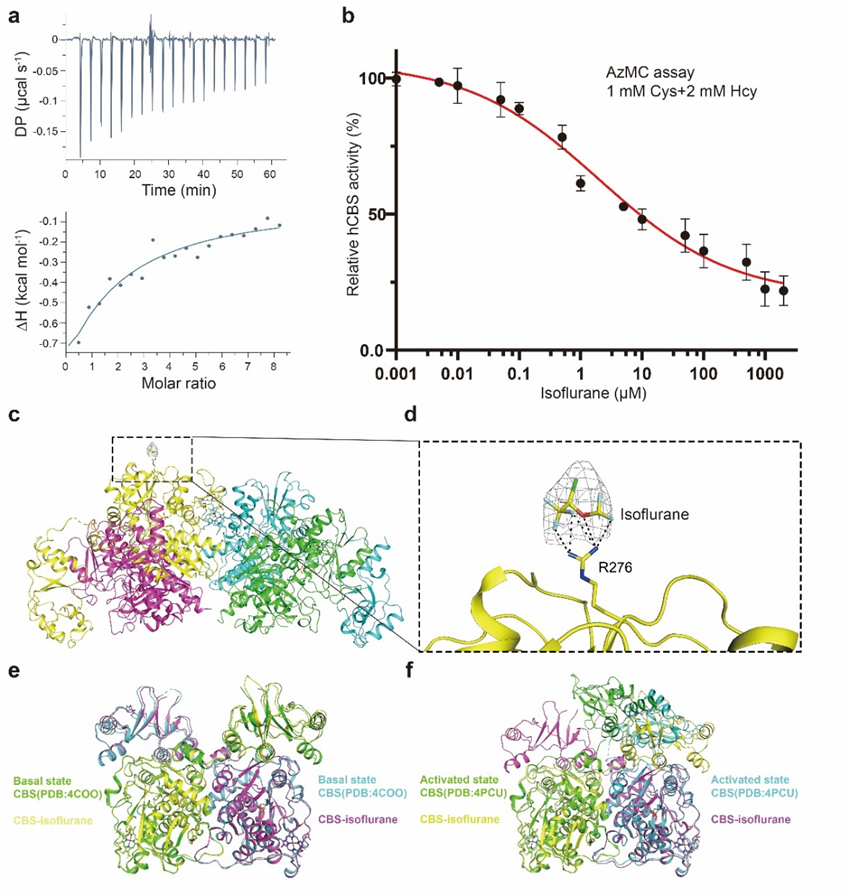
异氟烷结合CBS并抑制其活性的结构基础
综上所述,本研究揭示了异氟烷对成年和老年动物社交功能的影响,证实了CBS对社会行为的重要调控作用,并首次解析了异氟烷与CBS的结合位点,为理解麻醉药物作用的结构基础提供了新的见解。这些结果不仅能够为设计新型调控CBS活性的药物提供理论依据,还提示CBS可能是防治麻醉相关并发症的有前景的干预靶点。
同济大学附属上海市第四人民医院何梦凡博士、万晗曦博士后、丛培林博士后为本文第一作者。同济大学附属上海市第四人民医院熊利泽教授、许可教授、田莉教授为本文共同通讯作者。该研究主要得到国家自然科学基金重大项目、国家自然科学基金优秀青年科学基金和国家重点研发计划等资助。